 |
  Caractéristiques techniques Caractéristiques techniques
Pour chaque instrument, il existe des caractéristiques techniques qui permettent de
définir, en quelque sorte, une carte d'identité de l'appareillage.
En utilisant un monochromateur, on divise par deux la largeur de la raie d'excitation. Les spectres ainsi obtenus ont une meilleure résolution. La perte de puissance résultant de ce filtrage en énergie est compensée par une multi-détection. l'XPS permet de caractériser de petites surfaces sur une profondeur de quelques nanomètres. Excepté l'hydrogène, tous les éléments sont détectables.  Exploitation des résultats Exploitation des résultats
étude qualitative
Comme l'énonce Niels Bohr, chaque atome a une structure électronique ordonnée propre. Les électrons qui composent cette structure sont répartis sur des niveaux d'énergies définies. à titre d'exemple, dans la figure 1, le pic à 285 eV est caractéristique d'une famille d'électrons gravitant sur l'orbitale 1s du carbone. Un spectre général peut présenter plusieurs pics (niveaux d'énergie) d'un même atome (ex: Si2p, Si2s). Contrairement à l'idée reçue,l'intensité des pics ne permet pas d'estimer la part relative de chaque élément. Les liaisons chimiques Les éventuelles liaisons chimiques entre plusieurs éléments vont perturber l'ordre précédemment décrit (modèle de Bohr) ; les orbitales des atomes mis en jeu se déplacent en énergie. Ce phénomène s'observe sur le spectre et son amplitude dépend de la nature des liaisons chimiques créées. Chaque raie ainsi obtenue est la juxtaposition des différentes contributions chimiques. L'étude de leurs énergies permet d'établir la nature des liaisons formées. Reprenons l'exemple de la figure 1, représentatif d'un échantillon contenant du carbone et de l'oxygène. La liaison chimique entre ces deux atomes fait apparaêtre sur les raies O1s et C1s de nouvelles contributions. Les déplacements observés sont plus importants pour le carbone que pour l'oxygène, ce qui s'explique par la différence d'électronégativité de ces éléments. Pour un niveau donné (orbitale O1s dans le matériau), chaque voisin apportera ses contributions qui pourront être modélisées par des pics de forme gausso-lorentzienne. La figure 2 montre la décomposition des deux orbitales 1s dans le cas d'une liaison C-O. 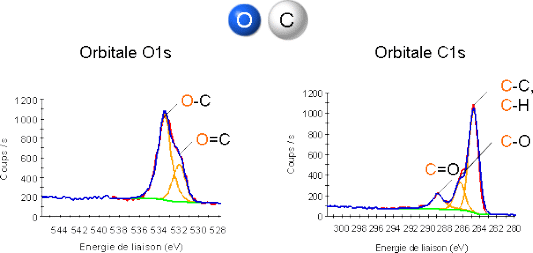  Modélisation des différentes contributions Modélisation des différentes contributions
Le rayonnement X utilisé pour irradier les matériaux est loin de ressembler à une
fonction de Dirac. On parle plutôt de raie d'excitation avec une distribution en énergie.
La forme de cette raie est Gaussienne. Elle est définie par sa largeur à mi-hauteur ou
FWHM -acronyme anglais de "Full Width Half Maximum"-, par sa position et son amplitude.
Selon la finesse de cette raie, le spectre de réponse sera plus ou moins bien résolu.
Rappelons que l'utilisation d'un monochromateur, dans le cas d'une source aluminium, va
permettre de réduire la largeur à mi-hauteur par un facteur 2.
La matière ne reste pas indifférente devant une source d'excitation. Selon sa nature chimique, elle va modifier le signal de sortie. En résumé, la réponse que l'on observe sur un spectre est le résultat d'une convolution entre la raie X, la réponse de la matière et la fonction de transfert de l'appareil. La conception des appareils avec un analyseur hémisphérique permet, en première approximation, de simplifier ces calculs induits par ces différentes fonctions.  étude quantitative étude quantitative
L'étape de quantification consiste à compter les électrons émis par les différents
constituants du matériau. Sans l'utilisation d'échantillons de référence,l'ensemble des
électrons collectés est considéré comme représentant 100% des constituants de l'échantillon.
Il s'agit donc d'une méthode de semi-quantification.
Par ailleurs, pour tenir compte des différents phénomènes d'interaction rayonnement/matière et électron/matière, on applique à ces données initiales, c'est-à-dire au nombre d'électrons collectés, des facteurs correctifs. On obtient finalement des pourcentages atomiques pour chacun des constituants. Cette étape ne permet pas de répondre à toutes les questions liées à l'étude des surfaces. Ainsi, on peut à juste titre se demander comment sont répartis ces éléments dans la zone analysée. La figure 3 présente quatre modèles de zones d'analyse comportant deux éléments répartis de manière différente. Ces quatre échantillons ont des surfaces aux propriétés physico-chimiques distinctes. Pourtant, d'un point de vue quantitatif, les résultats obtenus sont identiques : 20% de bleu et 80 % de gris. Il est donc nécessaire de compléter l'étude pour déterminer la répartition de ces éléments. L'analyse angulaire,l'étude du bruit de fond et les profils de concentration vont permettre de répondre à cette question.  L'XPS caractérise les éléments chimiques à la surface d'un échantillon. Cette technique détermine la nature des liaisons chimiques et quantifie la part de chacune de ces liaisons. |